Produkte
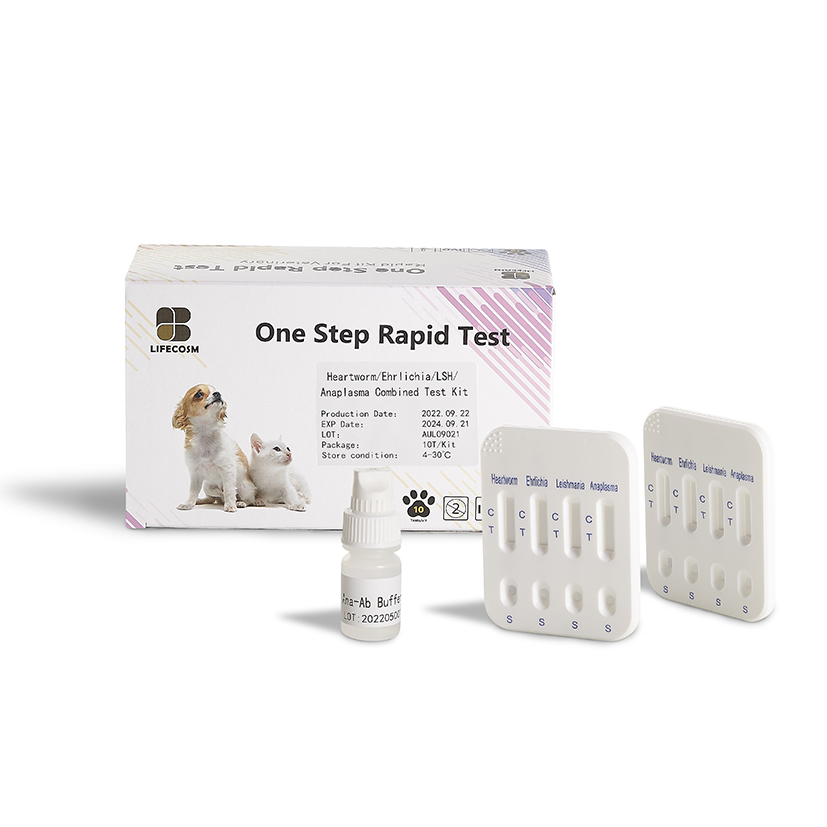
Lifecosm CHW Ag/Anaplasma Ab/E.canis Ab/LSH Ab Testkit
CHW Ag/Anaplasma Ab/E.canis Ab/LSH Ab Testkit Hundeherzwurm Ag/Anaplasma Ab /Ehrlichia canis Ab/Leishmania Ab Testkit
| Katalognummer | RC-CF31 |
| Zusammenfassung | Nachweis von Caninen Dirofilaria immitis-Antigenen, Anaplasma-Antikörpern, E. canis-Antikörpern und LSH-Antikörpern innerhalb von 10 Minuten |
| Prinzip | Einstufiger immunchromatographischer Test |
| Erkennungsziele | CHW Ag: Dirofilaria immitis-Antigene Anapalsma Ab: Anaplasma-AntikörperE. canis Ab: E. canis-Antikörper LSH Ab: L. chagasi, L. infantum und L. donovani Antiboys |
| Probe | Vollblut, Plasma oder Serum von Hunden |
| Lesezeit | 10 Minuten |
| Menge | 1 Karton (Kit) = 10 Geräte (Einzelverpackung) |
| Inhalt | Testkit, Pufferflasche und Einweg-Tropfer |
| Lagerung | Raumtemperatur (bei 2 ~ 30℃) |
| Ablauf | 24 Monate nach Herstellung |
| Vorsicht | Nach dem Öffnen innerhalb von 10 Minuten verbrauchenVerwenden Sie die entsprechende Probenmenge (0,01 ml einer Pipette). Bei kalter Lagerung nach 15–30 Minuten bei Raumtemperatur verwenden. Betrachten Sie die Testergebnisse nach 10 Minuten als ungültig |
Information
Erwachsene Herzwürmer werden mehrere Zentimeter lang und leben in den Lungenarterien, wo sie ausreichend Nährstoffe aufnehmen können. Die Herzwürmer in den Arterien lösen Entzündungen aus und bilden Hämatome. Das Herz muss dann häufiger pumpen als zuvor, da die Anzahl der Herzwürmer zunimmt und die Arterien verstopft.
Wenn sich die Infektion verschlimmert (bei einem 18 kg schweren Hund sind über 25 Herzwürmer vorhanden), wandern die Herzwürmer in den rechten Vorhof und blockieren den Blutfluss.
Wenn die Zahl der Herzwürmer mehr als 50 erreicht, könnten sie besetzen
Vorhöfe und Ventrikel.
Bei einer Infektion mit über 100 Herzwürmern im rechten Teil des Herzens verliert der Hund die Herzfunktion und stirbt schließlich. Diese tödliche
Dieses Phänomen wird als „Caval-Syndrom“ bezeichnet.
Im Gegensatz zu anderen Parasiten sind Herzwürmer kleine Insekten, sogenannte Mikrofilarien. Mikrofilarien von Mücken gelangen in Hunde, wenn diese Blut saugen. Die Herzwürmer, die zwei Jahre im Wirt überleben können, sterben ab, wenn sie innerhalb dieser Zeit nicht in einen anderen Wirt übergehen. Die Parasiten in einer trächtigen Hündin können deren Embryo infizieren.
Eine frühzeitige Untersuchung auf Herzwürmer ist sehr wichtig, um sie zu beseitigen. Herzwürmer durchlaufen mehrere Stadien wie L1, L2 und L3, einschließlich der Übertragung durch Mücken, bis sie zu erwachsenen Herzwürmern werden.
Herzwürmer in Mücken
Mikrofilarien in Mücken entwickeln sich innerhalb weniger Wochen zu Parasiten der Stufen L2 und L3, die Hunde infizieren können. Das Wachstum hängt vom Wetter ab. Die günstigste Temperatur für den Parasiten liegt über 13,9 °C.
Wenn ein Hund von einer infizierten Mücke gestochen wird, dringen Mikrofilarien der Stufe L3 in seine Haut ein. Dort entwickeln sich die Mikrofilarien innerhalb von 1 bis 2 Wochen zu L4. Nach drei Monaten in der Haut entwickelt sich L4 zu L5, das ins Blut gelangt.
L5 als Form des erwachsenen Herzwurms dringt in das Herz und die Lungenarterien ein, wo die Herzwürmer 5 bis 7 Monate später Insekten legen.


Diagnose
Bei der Diagnose des Hundes sollten die Krankheitsgeschichte und die klinischen Daten sowie verschiedene Diagnosemethoden berücksichtigt werden. Beispielsweise sind Röntgen-, Ultraschall- und Blutuntersuchungen, der Nachweis von Mikrofilarien und im schlimmsten Fall eine Autopsie erforderlich.
Serumuntersuchung;
Nachweis von Antikörpern oder Antigenen im Blut
Antigenuntersuchung;
Der Schwerpunkt liegt auf dem Nachweis spezifischer Antigene weiblicher adulter Herzwürmer. Die Untersuchung wird im Krankenhaus durchgeführt und weist eine hohe Erfolgsquote auf. Die handelsüblichen Testkits sind auf den Nachweis von 7–8 Monate alten adulten Herzwürmern ausgelegt, sodass Herzwürmer unter 5 Monaten schwer zu erkennen sind.
Behandlung
Eine Herzwurminfektion lässt sich in den meisten Fällen erfolgreich heilen. Um alle Herzwürmer zu beseitigen, ist die Einnahme von Medikamenten die beste Methode. Eine frühzeitige Erkennung der Herzwürmer erhöht die Erfolgschancen der Behandlung. Im Spätstadium der Infektion können jedoch Komplikationen auftreten, die die Behandlung erschweren.
Information
Das Bakterium Anaplasma phagocytophilum (früher Ehrilichia phagocytophila) kann bei verschiedenen Tierarten, einschließlich dem Menschen, Infektionen hervorrufen. Die Erkrankung bei Wiederkäuern wird auch als durch Zecken übertragenes Fieber (TBF) bezeichnet und ist seit mindestens 200 Jahren bekannt. Bakterien der Familie Anaplasmataceae sind gramnegative, unbewegliche, kokken- bis ellipsoide Organismen mit einem Durchmesser von 0,2 bis 2,0 µm. Sie sind obligat Aerobier ohne Glykolyseweg und alle sind obligate intrazelluläre Parasiten. Alle Arten der Gattung Anaplasma bewohnen membranausgekleidete Vakuolen in unreifen oder reifen hämatopoetischen Zellen von Säugetierwirten. Ein Phagocytophilum infiziert Neutrophile und der Begriff granulozytotrop bezieht sich auf infizierte Neutrophile. In seltenen Fällen wurden Organismen in Eosinophilen gefunden.
Anaplasma phagocytophilum
Symptome
Häufige klinische Anzeichen vonZu den Symptomen der caninen Anaplasmose zählen hohes Fieber, Lethargie, Depression und Polyarthritis. Auch neurologische Symptome (Ataxie, Krampfanfälle und Nackenschmerzen) können auftreten. Eine Infektion mit Anaplasma phagocytophilum verläuft selten tödlich, es sei denn, sie wird durch andere Infektionen kompliziert. Bei Lämmern wurden direkte Verluste, Verkrüppelungen und Produktionsverluste beobachtet. Bei Schafen und Rindern wurden Fehlgeburten und Störungen der Spermatogenese festgestellt. Die Schwere der Infektion wird von verschiedenen Faktoren beeinflusst, wie z. B. den beteiligten Varianten von Anaplasma phagocytophilum, anderen Krankheitserregern, Alter, Immunstatus und Zustand des Wirts sowie Faktoren wie Klima und Haltung. Es sollte erwähnt werden, dass die klinischen Manifestationen beim Menschen von einer leichten, von selbst verlaufenden grippeähnlichen Erkrankung bis hin zu einer lebensbedrohlichen Infektion reichen. Die meisten Infektionen beim Menschen führen jedoch wahrscheinlich nur zu minimalen oder keinen klinischen Manifestationen.
Übertragung
Anaplasma phagocytophilum wird durch Ixodes-Zecken übertragen. In den USA sind Ixodes scapularis und Ixodes pacificus die Hauptüberträger, während in Europa Ixode ricinus der wichtigste exophile Überträger ist. Anaplasma phagocytophilum wird von diesen Vektorzecken transstadial übertragen, und es gibt keine Hinweise auf eine transovarielle Übertragung. Die meisten bisherigen Studien zur Bedeutung von Säugetierwirten von A. phagocytophilum und seinen Zeckenvektoren konzentrierten sich auf Nagetiere. Dieser Organismus hat jedoch ein breites Wirtsspektrum unter Säugetieren und infiziert domestizierte Katzen, Hunde, Schafe, Kühe und Pferde.

Diagnose
Der indirekte Immunfluoreszenztest ist der wichtigste Test zum Nachweis einer Infektion. Serumproben aus der akuten und Rekonvaleszenzphase können auf eine vierfache Veränderung des Antikörpertiters gegen Anaplasma phagocytophilum untersucht werden. Intrazelluläre Einschlüsse (Morulea) werden in Granulozyten auf Wright- oder Gimsa-gefärbten Blutausstrichen sichtbar. Polymerase-Kettenreaktion (PCR)-Methoden werden zum Nachweis von Anaplasma phagocytophilum-DNA eingesetzt.
Verhütung
Es gibt keinen Impfstoff zur Vorbeugung einer Infektion mit Anaplasma phagocytophilum. Die Prävention beruht auf der Vermeidung des Kontakts mit dem Zeckenüberträger (Ixodes scapularis, Ixodes pacificus und Ixode ricinus) vom Frühjahr bis zum Herbst, der prophylaktischen Anwendung von Antiakariziden und der prophylaktischen Anwendung von Doxycyclin oder Tetracyclin bei Aufenthalten in Gebieten, in denen Ixodes scapularis, Ixodes pacificus und Ixode ricinus zeckenbefallen sind.
Information
Ehrlichia canis ist ein kleiner, stäbchenförmiger Parasit, der von der braunen Hundezecke (Rhipicephalus sanguineus) übertragen wird. E. canis ist der Erreger der klassischen Ehrlichiose bei Hunden. Hunde können mit verschiedenen Ehrlichia-Arten infiziert sein, die häufigste Ursache für Ehrlichiose ist jedoch E. canis.
Mittlerweile ist bekannt, dass sich E. canis in den gesamten Vereinigten Staaten, Europa, Südamerika, Asien und dem Mittelmeerraum verbreitet hat.
Infizierte Hunde, die nicht behandelt werden, können jahrelang asymptomatische Träger der Krankheit bleiben und schließlich an massiven Blutungen sterben.

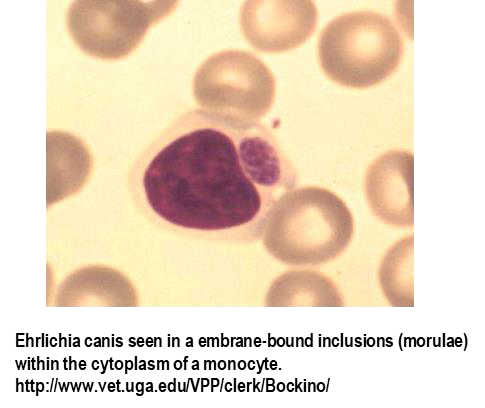
Symptome
Eine Infektion mit Ehrlichia canis bei Hunden verläuft in drei Stadien;
AKUTE PHASE: Dies ist in der Regel eine sehr milde Phase. Der Hund ist teilnahmslos, frisst nicht und kann geschwollene Lymphknoten haben. Fieber kann ebenfalls auftreten, aber selten führt diese Phase zum Tod. Die meisten Hunde regenerieren sich von selbst, manche treten jedoch in die nächste Phase ein.
SUBKLINISCHE PHASE: In dieser Phase erscheint der Hund normal. Der Organismus hat sich in der Milz eingeschlossen und versteckt sich dort.
CHRONISCHE PHASE: In dieser Phase erkrankt der Hund erneut. Bis zu 60 % der mit E. canis infizierten Hunde leiden aufgrund der verminderten Thrombozytenzahl an anormalen Blutungen. Durch die langfristige Immunstimulation kann es zu einer tiefen Augenentzündung (Uveitis) kommen. Auch neurologische Auswirkungen können auftreten.
Diagnose und Behandlung
Für die endgültige Diagnose von Ehrlichia canis sind die Visualisierung der Morula in Monozyten in der Zytologie, der Nachweis von E. canis-Serum-Antikörpern mit dem indirekten Immunfluoreszenz-Antikörpertest (IFA), die Amplifikation der Polymerase-Kettenreaktion (PCR) und/oder Gel-Blotting (Western-Immunoblotting) erforderlich.
Die wichtigste Maßnahme zur Vorbeugung der Ehrlichiose bei Hunden ist die Zeckenbekämpfung. Das Mittel der Wahl zur Behandlung aller Formen der Ehrlichiose ist Doxycyclin für mindestens einen Monat. Bei Hunden mit akuter oder leichter chronischer Erkrankung sollte innerhalb von 24 bis 48 Stunden nach Behandlungsbeginn eine deutliche klinische Besserung eintreten. Während dieser Zeit beginnt die Thrombozytenzahl zu steigen und sollte innerhalb von 14 Tagen nach Behandlungsbeginn wieder im Normalbereich liegen.
Nach einer Infektion ist eine erneute Infektion möglich; die Immunität nach einer früheren Infektion hält nicht an.
Verhütung
Die beste Vorbeugung gegen Ehrlichiose besteht darin, Hunde zeckenfrei zu halten. Dazu gehört die tägliche Untersuchung der Haut auf Zecken und die Behandlung von Hunden mit Zeckenschutzmitteln. Da Zecken andere verheerende Krankheiten wie Borreliose, Anaplasmose und Rocky-Mountain-Fleckfieber übertragen, ist es wichtig, Hunde zeckenfrei zu halten.
Information
Leishmaniose ist eine schwerwiegende parasitäre Erkrankung von Menschen, Hunden und Katzen. Der Erreger der Leishmaniose ist ein Protozoenparasit und gehört zum Leishmania-donovani-Komplex. Dieser Parasit ist in gemäßigten und subtropischen Ländern Südeuropas, Afrikas, Asiens, Südamerikas und Mittelamerikas weit verbreitet. Leishmania donovani infantum (L. infantum) ist für die Erkrankung bei Katzen und Hunden in Südeuropa, Afrika und Asien verantwortlich. Hunde-Leishmaniose ist eine schwere, fortschreitende systemische Erkrankung. Nicht alle Hunde entwickeln nach einer Infektion mit den Parasiten eine klinische Erkrankung. Die Entwicklung der klinischen Erkrankung hängt von der Art der Immunreaktion des einzelnen Tieres ab.
gegen die Parasiten.
Symptome
Bei Hunden
Bei Hunden können sowohl viszerale als auch kutane Manifestationen gleichzeitig auftreten; im Gegensatz zum Menschen werden keine getrennten kutanen und viszeralen Syndrome beobachtet. Die klinischen Symptome sind variabel und können anderen Infektionen ähneln. Auch asymptomatische Infektionen können auftreten. Typische viszerale Symptome sind Fieber (auch intermittierend), Anämie, Lymphadenopathie, Splenomegalie, Lethargie, verminderte Belastbarkeit, Gewichtsverlust und verminderter Appetit. Zu den selteneren viszeralen Symptomen zählen Durchfall, Erbrechen, Meläna, Glomerulonephritis, Leberversagen, Nasenbluten, Polyurie-Polydipsie, Niesen, Lahmheit (aufgrund von Polyarthritis oder Myositis), Aszites und chronische Kolitis.
In Feline
Katzen sind selten infiziert. Bei den meisten infizierten Katzen beschränken sich die Läsionen auf verkrustete Hautgeschwüre, die sich meist an Lippen, Nase, Augenlidern oder Ohrmuscheln befinden. Viszerale Läsionen und Symptome sind selten.
Lebenszyklus
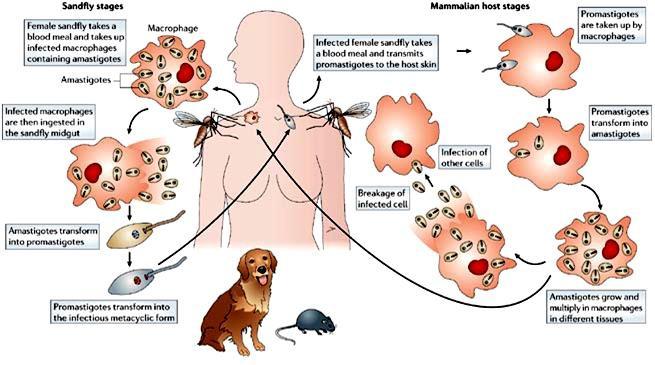
Der Lebenszyklus wird in zwei Wirten abgeschlossen. Einem Wirbeltierwirt und einem wirbellosen Wirt (Sandfliege). Die weibliche Sandfliege ernährt sich von Wirbeltierwirt undnimmt Amastigoten auf. Im Insekt entwickeln sich begeißelte Promastigoten. Die Promastigoten werden während der Nahrungsaufnahme der Sandmücke in den Wirbeltierwirt injiziert. Die Promastigoten entwickeln sich zu Amastigoten und vermehren sich hauptsächlich in den Makrophagen. Die Vermehrung in den Makrophagen der Haut, der Schleimhäute und der Eingeweide verursacht kutane, mukosale bzw. viszerale Leishmaniose.
Diagnose
Bei Hunden wird Leishmaniose üblicherweise durch direkte Beobachtung der Parasiten mittels Giemsa- oder proprietärer Schnellfärbung in Ausstrichen von Lymphknoten, Milz oder Knochenmarkaspiraten, Gewebebiopsien oder Hautabschabungen von Läsionen diagnostiziert. Organismen können auch in Augenläsionen, insbesondere in Granulomen, nachgewiesen werden. Die Amastigoten sind runde bis ovale Parasiten mit einem runden basophilen Kern und einem kleinen stäbchenförmigen Kinetoplasten. Sie kommen in Makrophagen vor oder werden aus rupturierten Zellen freigesetzt. Immunhistochemie und Polymerase-Kettenreaktion (PCR) werden ebenfalls eingesetzt.
Verhütung
Die am häufigsten eingesetzten Medikamente sind: Meglumin-Antimoniat in Kombination mit Allopurinol, Aminosidin und neuerdings auch Amphotericin B. Alle diese Medikamente erfordern eine Mehrfachdosis, die vom Zustand des Patienten und der Mitarbeit des Besitzers abhängt. Es wird empfohlen, die Erhaltungstherapie mit Allopurinol fortzusetzen, da ein Rückfall bei Hunden nach Absetzen nicht ausgeschlossen werden kann. Halsbänder mit Insektiziden, Shampoos oder Sprays zum wirksamen Schutz vor Sandmückenstichen müssen bei allen behandelten Patienten kontinuierlich angewendet werden. Die Vektorkontrolle ist einer der wichtigsten Aspekte der Krankheitskontrolle.
Die Sandmücke reagiert auf dieselben Insektizide wie der Malariaüberträger.